Матура по Химия 25 август 2025 ПП

Тук можете да решите варианта на матруата по химия от напълно безплатно онлайн.
На ваше разположение са помощни таблици, които можете да отворите като кликнете на заглавията долу. Първи модул можете да решите изцяло онлайн. Втори модул няма как да бъде точно оценен автоматично, за това сме ви подготвили въпросите в таблицата в ляво и отговорите в дясно. Решенията записвайте и след това проверете колко точки сте събрали. Скалта за оценяване можете да видите в дъното на страницата. Успех!
Първи модул
Първи модул е съставен от 30 задачи с един възможен отговор. Той може да бъде лесно оценен автоматично.
Втори модул
Характерът на задачите във втори модул прави изключително трудно невъзможно тяхното автоматично оценяване. Решете ги на лист, след което в решенията ще можете да сверите и точкувате задачите според указанието на МОН
1. Амониевият хлорид (нишадърът) е бяло кристално вещество, разтворимо във вода.
1.А. Изберете подходящите думи (ковалентни неполярни, ковалентни полярни, йонна, метална, делокализирана), с които могат да се характеризират химичните връзки в амониевия хлорид. Запишете отговора си в листа за отговори (втора част).
1.Б. Определете хибридното състояние на азотния атом в съединението.
2. В час по химия учител демонстрирал термичното разлагане на нишадър. Той поставил в суха чаша от веществото, затворил чашата с облодънна колба, пълна със студена вода, след което започнал да нагрява амониевия хлорид. Ученик от класа отразил вярно в протокола си наблюденията от експеримента (табл. 31.1.).

2.А. Като използвате данните от табл. 31.1, изразете с химично уравнение термичното разлагане на амониевия хлорид
2.Б. Изразете с люисови формули строежа на газовете X и Y. Определете кратността на връзките в молекулите им.
2.В. Запишете химичните уравнения, чрез които може да се обясни промяната в цвета на навлажнената лакмусовата хартия от X и Y.
2.Г. Изчислете ΔH° за разлагането на амониевия хлорид, като използвате следните стойности: ΔfH°(амониев хлорид) = –314,4 kJ/mol, ΔfH°(X) = –45,9 kJ/mol, ΔfH°(Y) = –92,3 kJ/mol. Определете дали процесът е екзо- или ендотермичен.
3. При определени условия (Т, p) в затворена система от т. 2 се установява химично равновесие.
3.А. Запишете израза за равновесната константа (Kc) на процеса.
3.Б. Протичането на коя реакция (правата/обратната) ще се благоприятства, ако:
3.Б.а. температурата се понижи;
3.Б.б. общото налягане се повиши (T = const)?
1. Ароматът на редица плодове, сред които и ягодите се дължи на комбинация от много
летливи съединения, но сред основните са естерите. Един от тях, който придава свеж и сладък
плодов аромат на ягодата може да се получи по схемата:
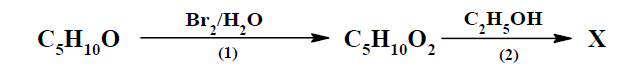
1.А. Изразете с химични уравнения преходите в схемата, ако е известно, че молекулите на
съединенията с молекулни формули C5H10O и C5H10O2 съдържат хирален (асиметричен)
въглероден атом. Напишете необходимите условия за протичане на реакция (2) и наименувайте
Х по IUPAC.
1.Б. Запишете полуреакциите за окислителя и редуктора в уравнение (1).
1.В. Какъв вид пространствена изомерия определя наличието на хирален въглероден атом в
молекулите на C5H10O и C5H10O2?
2. Естерът Y също допринася за аромата на ягодите. Той е верижен изомер на Х, получен от
етилов алкохол и съдържа киселинен остатък със същата дължина като Х, в който няма
хирален (асиметричен) въглероден атом.
2.А. Означете със съкратена структурна (или скелетна) формула Y.
2.Б. Колко mL етанол са необходими за естерификацията на съответната киселина, за да се
получат 19,5 g от Y? Подкрепете отговора си с подходящи изчисления. (За изчисленията
приемете, че: M(Y)=130,0 g/mol; M(С2Н5ОН)=46,0 g/mol; ρ(С2Н5ОН)=0,79 g/cm3).
2.В. Попълнете изречението с подходящите думи от речника, за да получите вярно твърдение за
естерите. Запишете избраните думи в листа за отговори (втора част).
Обикновено нискомолекулните алкилови естери притежават (1) по-слаба/по-голяма
способност да образуват водородни връзки с вода в сравнение с каброксилните киселини, от
които са получени, поради което имат (2) по-малка/по-голяма летливост от тях. Тези естери имат
характерен плодов аромат и често намират приложение в парфюмерийната и хранително-
вкусовата промишленост.
1. Медният сулфат е важно и широко използвано съединение в практиката. Безводната сол е
бяло кристално вещество, докато кристалохидратът на медния сулфат (CuSO4.5H2O) – син
камък, е с характерен син цвят, добре разтворим във вода.
1.А. Запишете съкратената или пълната електронна конфигурация на медните йони от състава на
синия камък.
1.Б. На какво се дължи синият цвят на кристалохидрата?
2. Разполагате с:
• железен пирон;
• водни разтвори на NaOH и BaCl2.
2.А. Запишете общото (сумарното) електронно-йонно уравнение, което доказва окислителните
свойства на катиона от разтвора на медния сулфат.
2.Б. Запишете съкратените йонни уравнения за доказване на катионите и анионите, съдържащи се в разтвор на син камък.
2.В. Изчислете молната концентрация на NaOH, при която ще започне образуването на съединението Х, доказващо катиона от разтвора на синия камък, ако молната концентрация на медните йони в него е 2,2.10─4 mol/L. (Ks(Х) = 2,2.10─20)
3. При разтваряне във вода синият камък хидролизира. Като приемете, че хидролизата е протекла напълно за всички медни йони:
3.А. Запишете съкратеното уравнение на хидролизата.
3.Б. Изчислете pH на разтвор на сярна киселина с молна концентрация 5.10─5 mol/L. Приемете, че при тази концентрация на киселината втората ѝ степен на дисоциация (α2) е 100%.
За първи път хипуровата киселина (от гръцки „hippos“ – кон) е открита в конската урина, откъдето произлиза името ѝ. Установено е, че киселината е един от крайните продукти на метаболизма на белтъците, както при повечето гръбначни животни, така и при човека. Този факт доказва способността на черния дроб да детоксикира ароматни съединения, попаднали в организма.
1. Съвременният синтез на хипурова киселина се основава на взаимодействието между бензоилхлорид и глицин (2-аминооцетна киселина) в основна среда (NaOH). Хипуровата киселина се изолира след добавяне на солна киселина.
1.А. Изразете с химично уравнение синтеза на киселината, като използвате съкратени структурни (или скелетни) формули. При реакцията се отделят също натриев хлорид и вода.
1.Б. Запишете наименованията на функционалните групи в молекулата на хипуровата киселина.
2. Най-голямо приложение хипуровата киселина намира в медицината като биомаркер. Повишените ѝ нива в урината са индикатор за системен контакт с толуен или бензоена киселина.
2.А. Означете със съкратени структурни (или скелетни) формули толуена и бензоената киселина.
2.Б. Към кой клас органични съединения принадлежи толуенът?
3. Работник в нефтопреработваща компания е бил изложен на толуен. В края на работния ден е събрана проба от 500 mL урина от работника, в която е отчетено съдържание на хипурова киселина с концентрация 0,02 mol/L.
3.А. Надвишена ли е стойността от максимално допустимите 3 g хипурова киселина в урината? Подкрепете извода си с подходящи изчисления. M(хипурова киселина) = 179 g/mol.
3.Б. Колко грама е абсорбирания от работника толуен (M(толуен) = 92 g/mol), ако 90% от него метаболизира до изчислената маса на хипуровата киселина от 3.А. Имайте предвид, че 1 mol толуен се преобразува в 1 mol хипурова киселина. Запишете резултата с цяло число.