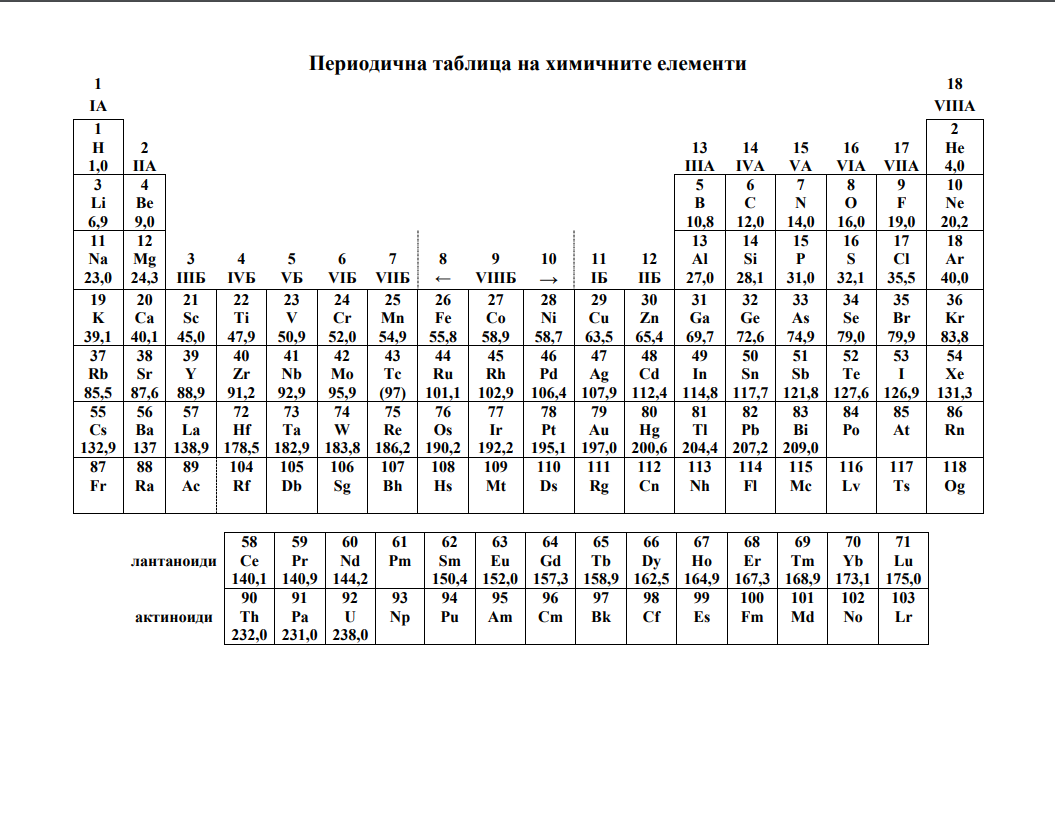
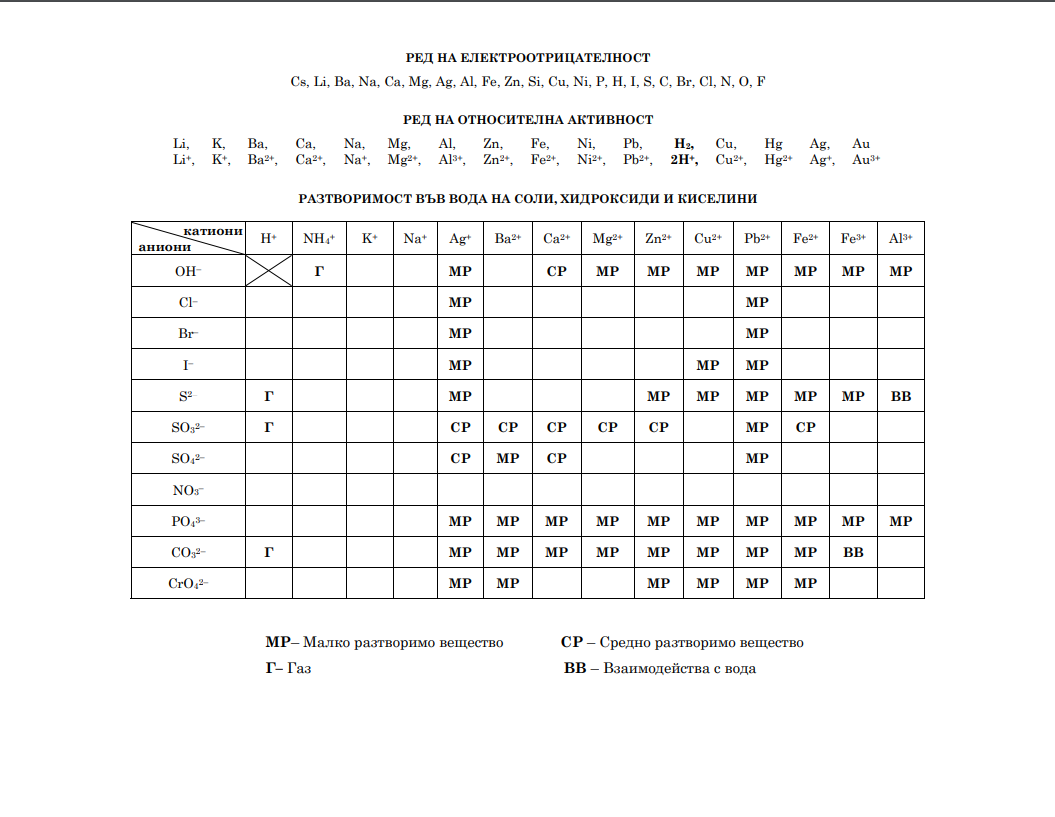
Матура по Химия 23 май 2025 ПП

Тук можете да решите варианта на матруата по химия от напълно безплатно онлайн.
На ваше разположение са помощни таблици, които можете да отворите като кликнете на заглавията долу. Първи модул можете да решите изцяло онлайн. Втори модул няма как да бъде точно оценен автоматично, за това сме ви подготвили въпросите в таблицата в ляво и отговорите в дясно. Решенията записвайте и след това проверете колко точки сте събрали. Скалта за оценяване можете да видите в дъното на страницата. Успех!
Първи модул
Първи модул е съставен от 30 задачи с един възможен отговор. Той може да бъде лесно оценен автоматично.
Втори модул
Характерът на задачите във втори модул прави изключително трудно невъзможно тяхното автоматично оценяване. Решете ги на лист, след което в решенията ще можете да сверите и точкувате задачите според указанието на МОН
Оксидите са едни от най-разпространените съединения на Земята. Те влизат в състава на хидросферата и на голяма част от литосферата.
1. Според свойствата си оксидите се разделят на основни, киселинни, амфотерни и неутрални. Дадени са формулите на следните оксиди: Al2O3, CaO, NO2, CO2, SO2, P2O3 и CO.
1.А. Кой от оксидите е неутрален? Запишете формулата му в листа за отговори.
1.Б. Кой от оксидите НЕ може да се получи при пряко взаимодействие на съответните прости вещества? Запишете формулата му в листа за отговори.
1.В. За кои от оксидите се отнасят твърденията:
А) Съответният му хидроксид намира приложение в строителството.
Б) Използва се в производството на силна киселина, която се съдържа в оловните акумулатори.
Запишете формулите на съответните оксиди в листа за отговори срещу буквите А) и Б).
2. Азотният диоксид се окислява от флуор по уравнението:
2NO2(г) + F2(г) → 2NO2F(г)
Установено е, че реакцията протича на два етапа:
1. етап (бавен): NO2(г) + F2(г) → NO2F(г) + F(г)
2. етап (бърз): NO2(г) + F(г) → NO2F(г)
2.А. Определете скоростоопределящия етап на реакцията. Запишете номера на избрания етап в листа за отговори.
2.Б. Запишете кинетичното уравнение на реакцията за скоростоопределящия етап.
2.В. Как може да се увеличи скоростта на реакцията на окисление на NO2 от флуор? Изберете възможните начини от предложените по-долу. Запишете съответните букви в листа за отговори.
А) Увеличаване на молната концентрация на NO2 четири пъти при постоянна температура.
Б) Понижаване на общото налягане при постоянна температура.
В) Увеличаване обема на реакционната смес при постоянна температура.
Г) Повишаване на температурата при постоянно налягане.
3. Серният диоксид се окислява до серен триоксид при повишена температура по уравнението
2SO2(г) + O2(г) ⇌ 2SO3(г). Процесът е екзотермичен, ускорява се от различни катализатори.
3.А. Определете вида на катализата, ако катализаторът е: (1) V2O5(тв); (2) NO(г).
В листа за отговори (втора част) срещу (1) и (2) запишете вида на катализата.
3.Б. При определени условия в системата се установява състояние на химично равновесие.
Напишете равновесната константа Kc на процеса.
3.В. Кои от изброените по-долу фактори водят до повишаване добива на продукта в тази
система.
В листа за отговори (втора част) запишете съответните букви.
А) понижаване на температурата
Б) внасяне на по-голямо количество катализатор
В) повишаване на налягането над реакционната смес
Г) повишаване на концентрацията на кислорода
Бензенът е най-простият представител на ароматните въглеводороди.
1. Всички въглеродни атоми в молекулата на бензена са в sp2-хибридно състояние. Молекулата му
е равнинна.
1.А. Определете вида на молекулата на бензена (полярна или неполярна). Запишете избраната
дума в листа за отговори.
1.Б. Изберете подходящите думи (йонна, ковалентна полярна, ковалентна неполярна,
координативна (донорно-акцепторна), π-делокализирана, метална, проста σ-), които се отнасят до
всички химични връзки в бензена. Запишете ги в листа за отговорите.
1.В. В кой от разтворителите (вода или хексан) бензенът има по-висока разтворимост при
25 ℃? Обяснете защо.
2. Бензенът е изходно вещество в следните превръщания:

2.А. Запишете със съкратени структурни (или скелетни) формули веществата А, Б и В, ако
знаете, че Б е вторичен алкилхалогенид. Преходите бензен → А и А → Б са реакции на
монозаместване.
2.Б. Определете вида (заместване, присъединяване, елиминиране) на органичните реакции. В
листа за отговори срещу номера на всяка реакция запишете вида ѝ.
3. Тривиалното наименование на съединението В е стирен. Едно от приложенията му е за получаване на полимера полистирен.
3.А. С кои два от изброените реактиви може да се докаже стиренът?
А) бромна вода
Б) реактив на Толенс – [Ag(NH3)2]OH
В) воден разтвор на FeCl3
Г) разреден воден разтвор на KMnO4
Запишете съответните букви в листа за отговори.
3.Б. Запишете със съкратена структурна (или скелетна) формула полимера полистирен
Газът азот има ниска химическа активност, но образува разнообразни съединения.
1. Хидразинът N2H4 е съединение на азота, което се използва като ракетно гориво. Гори с отделяне на голямо количество топлина по уравнението:
N2H4(г) + О2(г) → N2(г) + 2H2O(г) ΔH = –625,5 kJ/ mol
1.A. Определете хибридното състояние на азотните атоми в молекулата на хидразина:
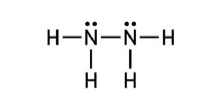
1.Б. Изчислете изменението на енталпията (в kJ) при изгаряне на 3,2 g хидразин. Резултатът закръглете до първия знак след десетичната запетая.
2. Азотистата киселина HNO2 е слаба киселина, която съществува само във воден разтвор.
2.А. Запишете химичното уравнение на протолитното равновесие, в което участва азотистата киселина. Запишете израза за протолитната ѝ константа.
2.Б. Изчислете pH на разтвор на азотиста киселина, в който молната концентрация на H3O+ е 1,0.10–5 mol/L.
3. Азотната киселина е едно от най-важните съединения на азота. В лабораторната практика се използва за разтваряне на някои малкоразтворими сулфиди.
В табл. 33.1. са представени данни за произведението на разтворимост Ks на някои сулфиди.

3.A. Коя от солите в табл. 33.1. има най-малка разтворимост във вода? В листа за отговори напишете формулата на съответния сулфид.
3.Б. Приготвени са наситени водни разтвори на сулфидите от табл. 33.1. при 25 ℃. В кой от тях равновесната молна концентрация на S2– е най-висока? В листа за отговори напишете формулата на съответния сулфид.
3.В. Медният сулфид се разтваря частично в топла разредена азотна киселина. При реакцията се получават меден(II) нитрат, сяра, азотен(II) оксид и вода. Запишете химичното уравнение на описания процес. Изравнете уравнението чрез метода на електронния баланс.
Малеиновата киселина е ненаситена дикарбоксилна киселина с относителна молекулна маса 116.
1. Малеиновата киселина съдържа само елементите въглерод, водород и кислород. В една молекула от тази киселина има четири водородни и четири кислородни атома. Определете молекулната формула на малеиновата киселина. Подкрепете отговора си с изчисления. (Ar(C) = 12,0; Ar(H) = 1,0; Ar(O) = 16,0).
2. Малеиновата киселина е (Z)-изомерът (cis-изомер) на ненаситената дикарбоксилна киселина. Запишете формулата на малеиновата киселина, като изразите пространственото разположение на заместителите при двойната връзка.
3. π-Диастереомерът на малеиновата киселина се нарича фумарова киселина. Двете киселини се различават съществено по свойства. В табл. 34.1. са дадени характерни константи за двете киселини.