Матура по Химия 27 август 2021
Тук можете да решите варианта на матруата по химия от 27 аегуст 2021 година.
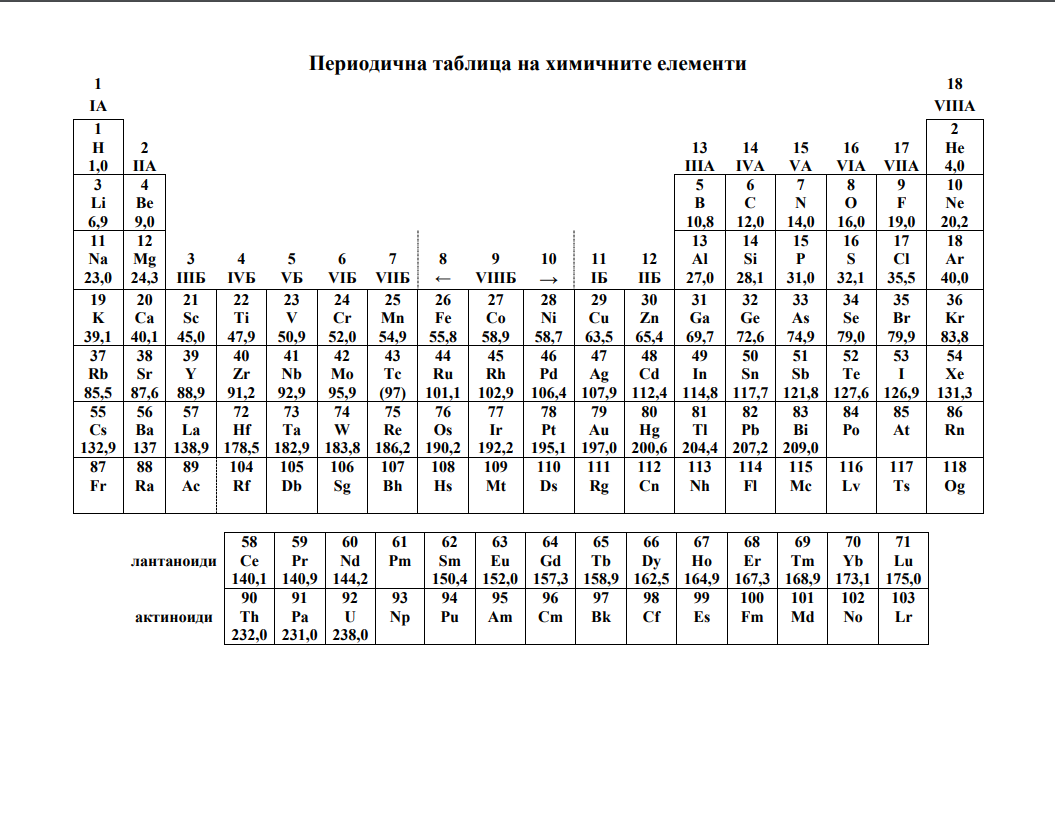
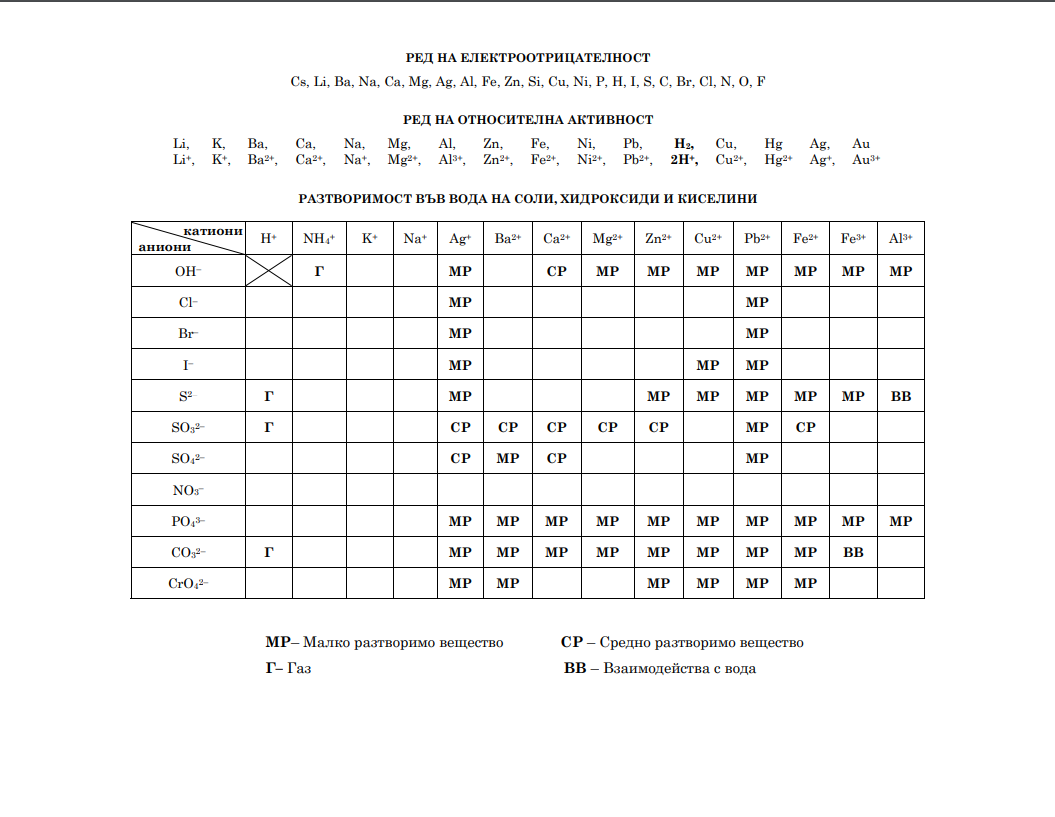
На ваше разположение са помощни таблици, които можете да отворите като кликнете на заглавията долу. Първи модул можете да решите изцяло онлайн. Втори модул няма как да бъде точно оценен автоматично, за това сме ви подготвили въпросите в таблицата в ляво и отговорите в дясно. Решенията записвайте и след това проверете колко точки сте събрали.
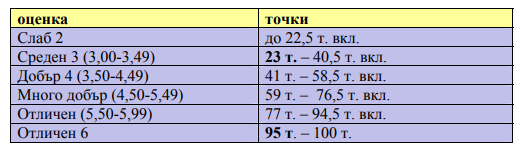
Схемата за оценяване можете да видите в дъното на страницата. Успех!
ПЪРВИ МОДУЛ
Модулът съдържа 35 затворени въпроса с по един възможен отговор. Поради това, този раздел може да бъде оценен автоматично. За всеки верен отговор получавте по една точка. Максимално можете да изкарате 35 точки.Решете теста, запомнете получения брой точки и преминете към втори модул.
ВТОРИ МОДУЛ
Втори модул съдържа задачи с отворен отговор. Тях ще трябва да решите на лист и да оцените самостоятелно според дадения критерий. Запомнене броя точки от първи модул и добавяйте указания брой точки за всеки верен отговор.Мкасималният брой точки, който можете да получите е 65 т.
За вашата подготовка е най-полезно да дадете вашите отговори преди да започнете да проверявате решенията и да точкувате.
Въпроси
36. Химичният елемент Е се намира в трети период на Периодичната таблица. Простото му вещество е в твърдо агрегатно състояние с жълт цвят. Привзаимодействието му с водород се получава газообразно вещество с неприятна
миризма.
А) Напишете наименованието на химичния елемент Е.
Б) Запишете химичната формула на газообразното вещество, получено привзаимодействие на простото вещество на елемента Е с водород, като заместите Е с химичния знак на елемента.
В) Какъв е характерът на водния разтвор на водородното съединение на химичния елемент Е?
37. Амониевият хлорид, известен още като нишадър, се използва за почистване наметални повърхности преди нанасяне на антикорозионни покрития. Термичното му разлагане е обратим процес. При висока температура амониевият хлорид се разлага до амоняк и хлороводород, а при стайна температура смес от двата газа образува твърд амониев хлорид.
А) Изразете с химично уравнение термичното разлагане на нишадъра.
Б) Ако системата е в състояние на химично равновесие опишете как ще се промени количеството на амониевия хлорид, ако се повиши температурата.
38. За лабораторна работа са необходими разтвори на сребърен нитрат и на натриев хлорид.
А) Изчислете колко грама твърд AgNO3 са необходими за приготвянето на 500 mL разтвор на сребърен нитрат с молна концентрация c(AgNO3) = 0,1 mol/L. Mолната маса на солта е M(AgNO3) = 170 g/mol.
Б) Колко грама вода са необходими за приготвяне на 800 g разтвор на натриев хлорид смасова част w(NaCl) = 2 %?
39. На етажерка в химическа лаборатория се намират еднакви стъкленици пълнис водни разтвори на NH3 и на CH3COOH.
А) В кой от двата разтвора концентрацията на хидроксидните йони (ОН–) е по-голяма?
Б) В кой от двата разтвора цветът на универсалния индикатор ще се промени в червен?
В) Ще нарасне или ще намалее стойността на рН на разтвора на NH3, ако към него седобави от разтвора на CH3COOH?
40. За всяко наименование от колона I посочете съответстващата му формула в колона II.
(В свитъка за свободните отговори срещу буквата А, Б, В и Г на наименованията, запишете цифрата от 1 до 7 за съответната формула.)

41. Съединенията на химичния елемент Х оцветяват пламъка в керемиденочервен цвят. Простото му вещество взаимодейства с кислорода и образува оксид ХО,известен в практиката като негасена вар. Оксидът взаимодейства с вода и при прибавяне на фенолфталеин към разтвора, той променя цвета си в малиновочервено.
А) Изразете с химично уравнение описания процес на получаване на оксида XO, като замените Х с химичния знак на елемента.
Б) Запишете с химично уравнение взаимодействието на оксида XO с вода, като замените Х с химичния знак на елемента. Каква е стойността на рН в получения разтвор ? (по-малка, по-голяма или равна на 7)
В) Запишете химичната формула на сол на елемента Х, която се използва в медицината при счупване на крайници.
42. Генетичен преход е изразен чрез схемата:
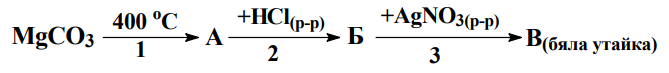
Изразете с химични уравнения процесите 1, 2 и 3, като заместите буквите А, Б и В сформулите на съответните съединения.
43. Кои от твърденията сa верни и кои – неверни? (В свитъка за свободните
отговори срещу буквите от А до Е запишете ДА или НЕ.)
А) Съединенията на елемента мед са отровни.
Б) Стомашният сок има рН > 7.
В) С въглероден оксид могат да се газират напитки.
Г) Магнезиеви йони се съдържат в хлорофила.
Д) Графитът е електропроводим.
Е) При непълно горене на въглища се получава въглероден оксид
44. За всяко наименование в колона I посочете съответстващата му формула вколона II. (В свитъка за свободните отговори срещу буквата А, Б, В и Г на наименованията, запишете цифрата от 1 до 7 за съответната формула.)

45. Дадени са структурните формули на шест органични съединения 1, 2, 3, 4, 5 и 6.
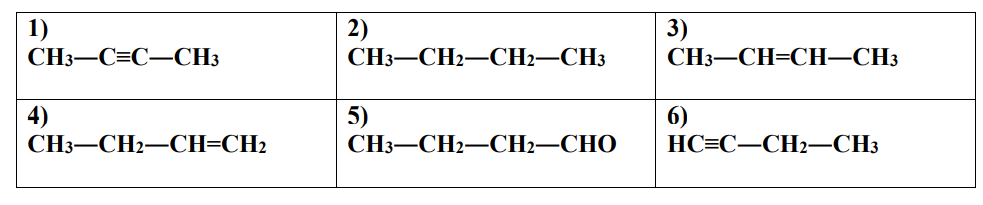
А) Кои две от съединенията са изомери с обща формула C4H6? (В свитъка за свободните отговори запишете номерата им.)
Б) Към кой хомоложен ред принадлежат съединенията от подточка А?
В) Запишете с молекулна формула техен хомолог, чиято молекула има с единвъглероден атом повече.
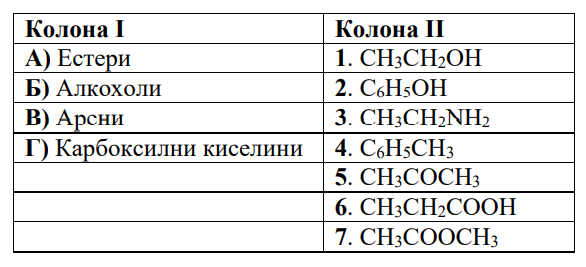
46. За всеки клас органични вещества от колона I изберете подходящ пример от
колона II. (В свитъка за свободните отговори срещу буквата А, Б, В и Г запишете с число от 1 до 7 номера на съответната формула от колона II.)
47. Фенолът е твърдо кристално вещество, което на въздуха лесно се окислява, като получените вещества са с розов цвят. Водните разтвори на фенола са използвани в миналото за дезинфекция.
А) Изразете с химично уравнение електролитната дисоциация на фенол във воденразтвор.
Б) Изразете с изравнено химично уравнение взаимодействието на фенол с натриева основа.
В) С кой реактив можете да докажете наличието на фенол в отпадни води? Как ще се оцвети разтворът?
48. Изразете с химични уравнения процесите 1, 2 и 3 в прехода, като заместитебуквите А, Б и В с формулите на съответните съединения:
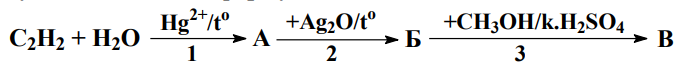
49. Липсващите в текста думи и изрази (1), (2) и (3) запишете в свитъка засвободните отговори, като изберете от следните:
озона, сярата, калция, азота,
замърсяване, увеличаване, обогатяване.
Дъждовната вода дори в най-чистата атмосфера има слабо киселинен характер (рН=5,6-5,7) поради присъствието на въглероден диоксид във въздуха. При наличието на оксиди на …(1)… и …(2)…, отделящи се при човешката дейност, киселинността на дъждовете
може да нарасне. Последствията са свързани с/със …(3)… на почви и води.
50. На графиката е показана зависимостта на разтворимостта на различни вещества от температурата.
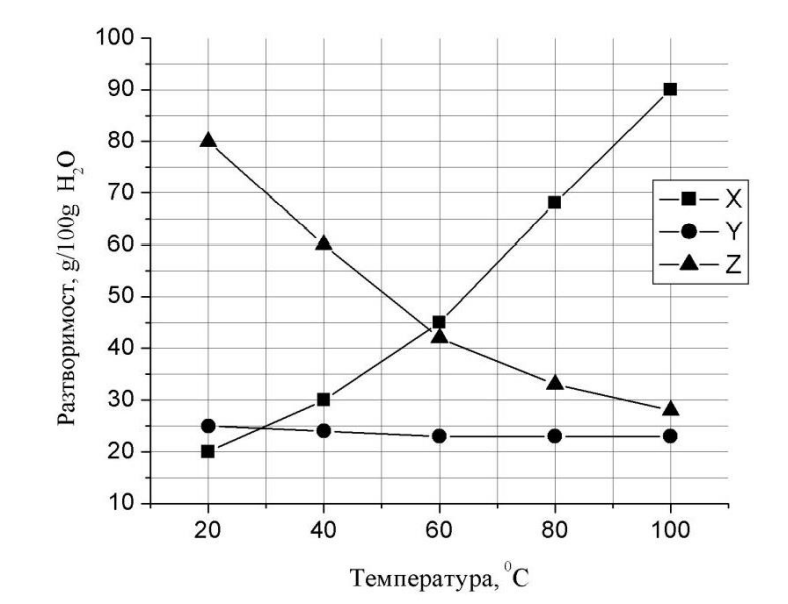
Използвайки графиката, определете:
А) Кое от веществата X, Y или Z има най-голяма разтворимост при 20 ℃?
Б) Разтворимостта на кое вещество се променя най-малко с промяна на температурата?
В) При 80 ℃ в две различни стъкленици с по 100 g вода са поставени по 50 g отвеществата X и Y. Кое от посочените вещества се е разтворило напълно? Определете вида на неговия разтвор (ненаситен, наситен, преситен).
Правилни отговори и точки
А) сяра – 1 т.
Б) H2S – 1 т.
В) киселинен – 1 т.
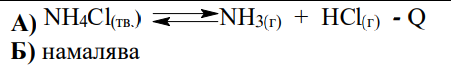
А) 2 т.
Б) 1 т.
А) n(AgNO3) = 0,05 mol – 1 т.
m(AgNO3) = 8,5 g – 1 т.
Б) m(NaCl) = 16 g – 1 т.
m(H2O) = 784 g – 1 т.
А) в разтвора на NH3 – 1 т.
Б) в разтвора на CH3COOH – 1 т.
В) ще намалее – 1 т.
А) – 5 – 1 т.
Б) – 3 – 1 т.
В) – 7 – 1 т.
Г) – 2 – 1 т.
A) 2Сa + O2 → 2СаO – 2 т.
Б) СаO + H2O → Сa(OH)2 – 2 т.
рН >7 – 1 т.
В) CaSO- 1 т.
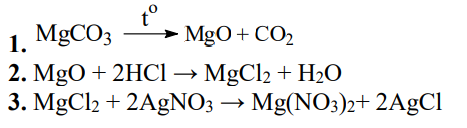
– 3 х 2 т..
А) Да – 1 т.
Б) Не – 1 т.
В) Не – 1 т.
Г) Да – 1 т.
Д) Да – 1 т.
Е) Да- 1 т.
А) – 5 – 1 т.
Б) – 7 – 1 т.
В) – 3 – 1 т.
Г) – 1 – 1 т.
А) 1 и 6 – 1 т.
Б) алкини – 1 т.
В) С5Н8 – 1 т.
А) – 7- 1 т.
Б) – 1 – 1 т.
В) – 4 – 1 т.
Г) – 6 – 1 т.
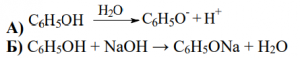
В) воден разтвор на FeCl3; синьо-виолетово
оцветяване
3 х 2 т.
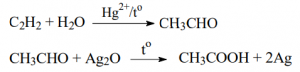
![]()
3 х 2 т.
(1) – сярата/азота – 1 т.
(2) – азота/сярата – 1 т.
(3) – замърсяване – 1 т.
А) Z – 1 т.
Б) Y – 1 т.
В) X, ненаситен – 2 х 1 т.
Резултат
Сега е момента да направите изчислението. Максималният брой точки от първи модул е 35 а от втори 65 точки.
Към поучените от вас товки от първата част доббавете точките от втората, която решихте на лист. Сравнете с таблицата в дясно. Тя е официалната таблица за оценяване на МОН.
Доволни ли сте от получения резултат?