Матура по Химия 31 май 2021
Тук можете да решите варианта на матруата по химия от 31 май 2021 година.
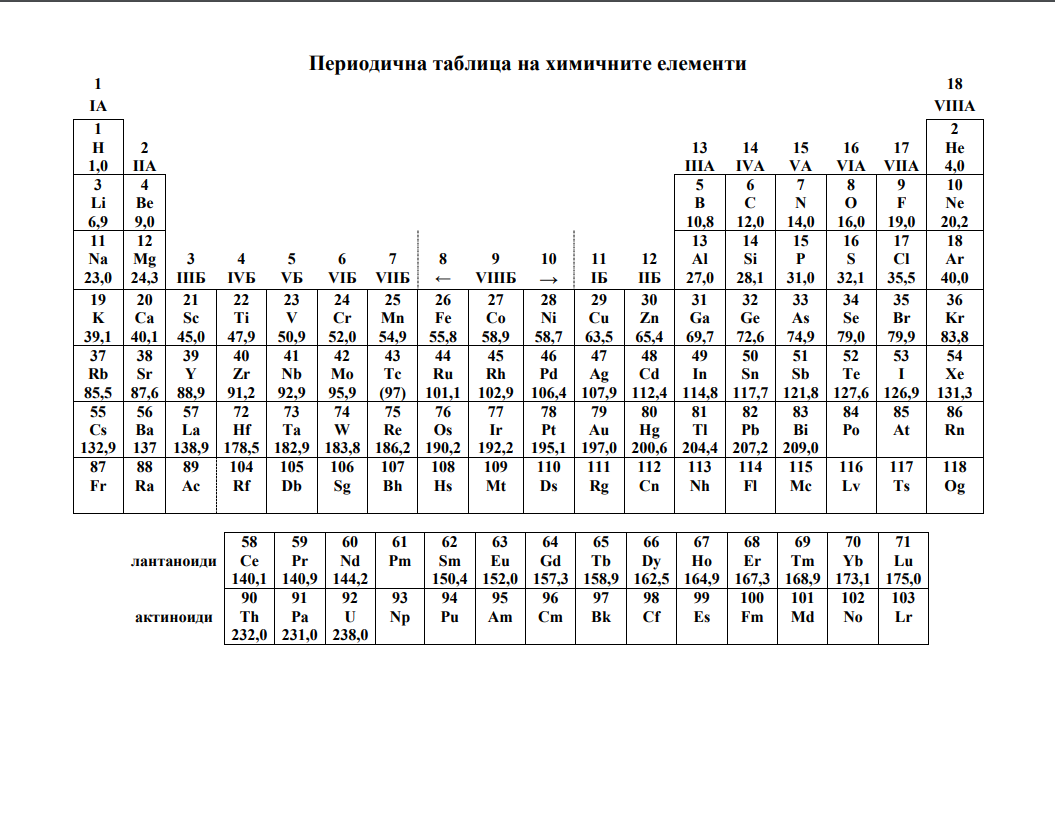
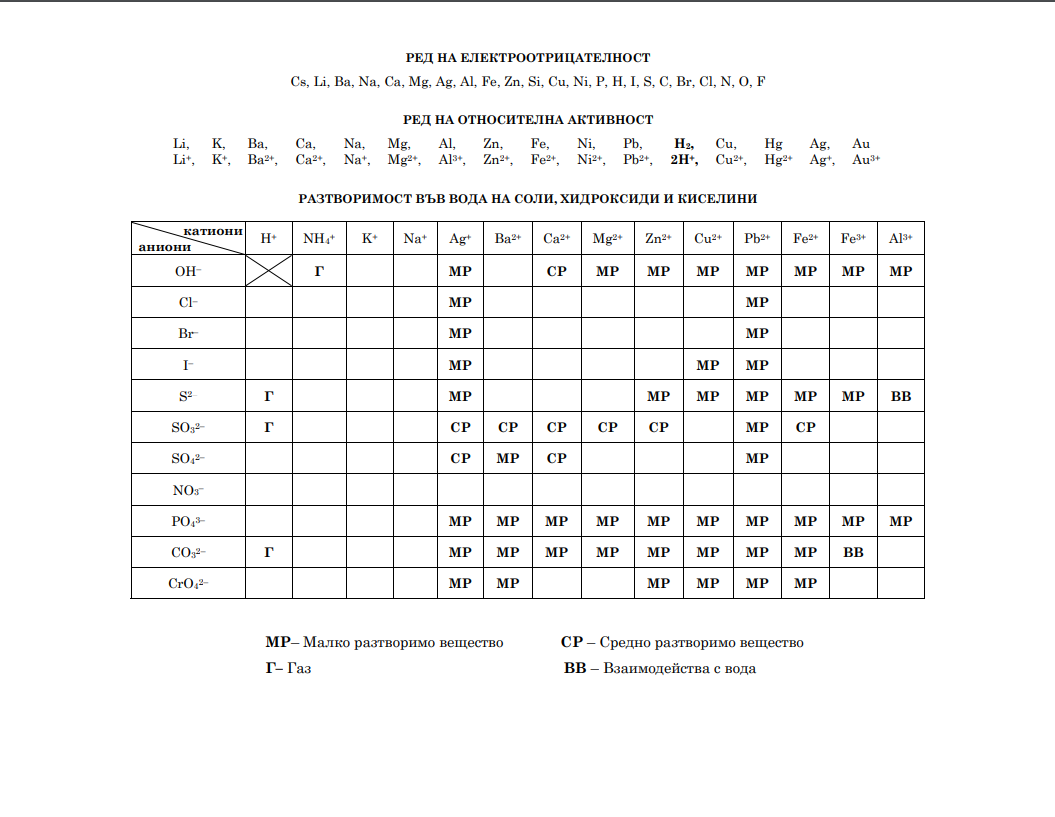
На ваше разположение са помощни таблици, които можете да отворите като кликнете на заглавията долу. Първи модул можете да решите изцяло онлайн. Втори модул няма как да бъде точно оценен автоматично, за това сме ви подготвили въпросите в таблицата в ляво и отговорите в дясно. Решенията записвайте и след това проверете колко точки сте събрали.
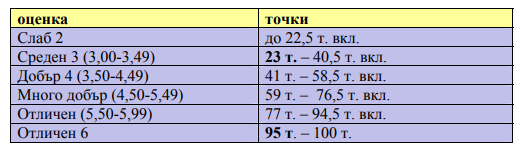
Схемата за оценяване можете да видите в дъното на страницата. Успех!
ПЪРВИ МОДУЛ
Модулът съдържа 35 затворени въпроса с по един възможен отговор. Поради това, този раздел може да бъде оценен автоматично. За всеки верен отговор получавте по една точка. Максимално можете да изкарате 35 точки.Решете теста, запомнете получения брой точки и преминете към втори модул.
ВТОРИ МОДУЛ
Втори модул съдържа задачи с отворен отговор. Тях ще трябва да решите на лист и да оцените самостоятелно според дадения критерий. Запомнене броя точки от първи модул и добавяйте указания брой точки за всеки верен отговор.Мкасималният брой точки, който можете да получите е 65 т.
За вашата подготовка е най-полезно да дадете вашите отговори преди да започнете да проверявате решенията и да точкувате.
Въпроси
36. При термично разлагане на варовик се получават два оксида – оксид А и оксид Б. Оксид А е известен като негасена вар, а водният разтвор на оксид Б променя цвета на виолетовия лакмус в червен.
А) Напишете формулата на варовика.
Б) Какъв химичен характер има оксид А?
В) На кои йони се дължи оцветяването на лакмуса във водния разтвор на веществото Б?
37. При прескачане на електрична искра в смес от азот и кислород се образува азотен оксид. Синтезът на азотен оксид протича по химичното уравнение:
N2(г) + O2(г) <–> 2NO(г) − Q
При определени условия в системата се установява равновесие.
А) Как ще се промени добивът на продукта при повишаване на налягането в равновесната система? (повишава се, намалява, не се променя)
Б) Как ще се промени добивът на продукта при повишаване на температурата? (повишава се, намалява, не се променя)
В) Как ще се промени равновесната концентрация на кислорода, ако се увеличи
концентрацията на азота? (повишава се, намалява, не се променя)
38. За приготвяне на кисело зеле се използва солен разтвор с масова част w (NaCl) = 4%.
А) Колко грама сол и колко грама вода са необходими за получаване на 1000 g солен разтвор
с масова част на солта 4%?
Б) Колко грама вода трябва да се добави към наличния солен разтвор, за да се получи нов
разтвор с масова част 2%?
39. В химичната лаборатория Иван разполага с два съда, в които има равни обеми на разтвори с различна стойност на рН − разтвор I и разтвор II.
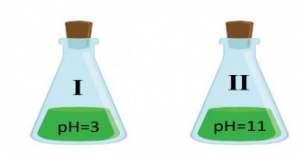
А) В кой от тях концентрацията на хидроксидните йони е по-голяма?
Б) Иван потапя късчета виолетовата лакмусова хартия в двата разтвора. В кой от тях цветът ѝ ще се промени в червен?
В) Как ще се промени pH в разтвор II, ако Иван прибави разтвор I към него? (ще се увеличи, ще намалее, няма да се промени)
40. Кои са липсващите формули и наименования А, Б, В и Г?
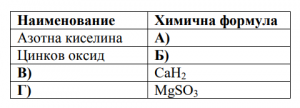
41. Изразете с изравнени молекулни химични уравнения следните процеси:
А) взаимодействие на натриева основа и сярна киселина
Б) взаимодействие на калциев оксид и вода
В) При един от процесите се получава продукт, който се използва в строителството и вселското стопанство. Запишете наименованието на това вещество.
Г) Как се нарича реакцията, описана в т. А)?
42. Изразете с химични уравнения прехода:
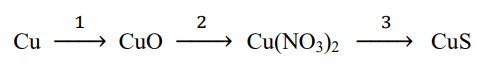
43. Кои от твърденията са верни и кои – неверни?
(В свитъка за отговори срещу буквите от А до Е запишете ДА или НЕ.)
А) Въглеродният диоксид се използва за производството на газирани напитки.
Б) Стомашният сок има рН > 7.
В) „Твърдостта“ на водата се определя от наличието на Cu2+ йони.
Г) Дървесната пепел може да се използва като минерален тор.
Д) Диамантът е електропроводник.
Е) Алуминият се използва за изработване на домакински съдове.
44. За всяко наименование от колона I посочете съответстващата му химична формулав колона II.
(В свитъка за свободните отговори срещу буквата А, Б, В и Гнанаименованията, запишете цифрата от 1 до 6 за съответната формула.)
45. Дадени са съединенията:

А) От съединенията от (1) до (6) посочете двойките изомери.
Б) Кои от тях са верижни изомери?
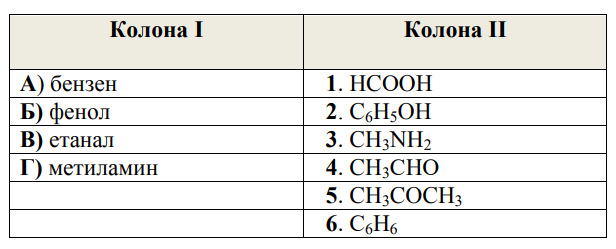
46. За всеки вид органични съединения от колона I посочете формула на съответенпредставител от колона II. (В свитъка за свободните отговори срещу буквата А, Б, В и Г на наименованията, запишете цифрата от 1 до 6 за съответната формула.)
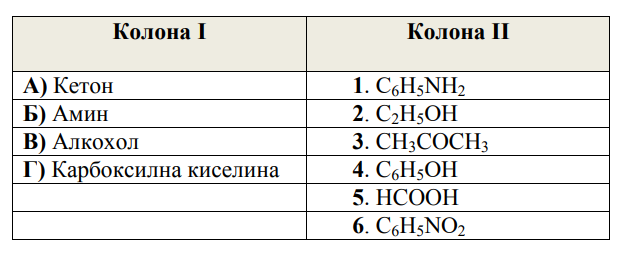
47. Две от означените взаимодействия са възможни.
(1) CH3CHO + Ag2O→
(2) CH3COCH3 + Cu(OH)2 →
(3) C6H5OH + HCl →
(4) CH4 + Cl2 →
А) Запишете с химични уравнения възможните процеси.
Б) Продуктът на една от възможните реакции се използва като консервант в хранително-вкусовата промишленост. Запишете наименованието му.
В) Определете вида на другата възможна реакция.
48. Дадени са преходите:
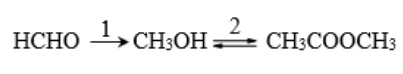
А) Изразете процесите 1 и 2 с химични уравнения.
Б) Определете вида на реакция 1.
В) Определете вида на реакция 2.
49. Запишете в свитъка за свободни отговори липсващите думи и изрази (1), (2) и (3),като изберете от:
литосферата, пещерни дупки, атмосферата, хидросферата, черни
дупки, фреоните, озонови дупки, въглеродния диоксид, феромоните.
Метеорологичните изследвания на озоновия слой показват, че на някои места в …(1)…,съдържанието на озон намалява. Тези места с нарушена концентрация на озона са наречени …(2)… . Има много хипотези за тяхното появяване. Една от тях е свързана с отрицателното въздействие на …(3)… върху озона.
(Отговорите запишете с число и избраната дума или израз срещу него.)
50. В две епруветки са поставени разтвори на веществата А и Б. Иван има за задача да разпознае веществата. Установил, че при внасяне в пламък веществото А го оцветява в жълто. Със сребърен нитрат веществото Б образува бяла утайка. Разтвор навеществото Б оцветява виолетовия лакмус в червено. При смесване на двете вещества
Иван установил, че се отделя газ с характерен шум. Кои са вещества А и Б?
(Отговорите запишете с буква и формулата на съответното вещество.)
Правилни отговори и точки
А) CaCO3 – 1 т.
Б) основен – 1 т.
В) на водородните положителни йони, H+ – 1 т.
А) не се променя – 1 т.
Б) повишава се – 1 т.
В) намалява – 1 т.
А ) m(NaCl) = 40 g – 1 т.
m(H2O) = 960 g – 1 т.
Б) m(H2O добавена) = 1000 g – 2 т.
А) в разтвор II – 1 т.
Б) в разтвор I – 1 т.
В) ще намалее – 1 т.
А) – HNO3 – 1 т.
Б) – ZnO – 1 т.
В) – калциев дихидрид – 1 т.
Г) – магнезиев сулфит – 1 т.
А) 2NaOH + H2SO4 → Na2SO4 + 2H2O – 2 т.
Б) CaO + H2O → Ca(OH)2 – 2 т.
В) гасена вар, калциев дихидроксид – 1 т.
Г) неутрализация – 1 т.
1. 2Cu + O2 → 2CuO – 2 т.
2. CuO + 2HNO3 → Cu(NO3)2 + H2O – 2 т.
3. Cu(NO3)2 + Na2S → CuS↓ + 2NaNO3 – 2 т.
А) Да – 1 т.
Б) Не – 1 т.
В) Не – 1 т.
Г) Да – 1 т.
Д) Не – 1 т.
Е) Да- 1 т.
А) – 6 – 1 т.
Б) – 2 – 1 т.
В) – 4 – 1 т.
Г) – 3 – 1 т.
А) 1 и 5; 2 и 4 – 2 х 1 т.
Б) 1 и 5 са верижни изомери – 1 т.
А) – 3 – 1 т.
Б) – 1 – 1 т.
В) – 2 – 1 т.
Г) – 5 – 1 т.
А) CH3CHO + Ag2O → CH3COOH + 2Ag
CH4 + Cl2 → CH3Cl + HCl – 2 х 1 т.
Б) CH3COOH, етанова киселина, оцетна киселина 1 т.
В) заместителна, халогениране 1 т.
А)
1. HCHO + H2 → CH3OH – 2 т.
2. CH3COOH + CH3OH CH3COOCH3 + H2O – 2 т.
Б) присъединителна реакция, хидриране – 1 т.
В) естерификация – 1 т.
(1) – атмосферата – 1 т.
(2) – озонови дупки – 1 т.
(3) – фреоните – 1 т.
А – Na2CO3, NaHCO3 – 2 т.
Б – HCl – 2 т.
Резултат
Сега е момента да направите изчислението. Максималният брой точки от първи модул е 35 а от втори 65 точки.
Към поучените от вас товки от първата част доббавете точките от втората, която решихте на лист. Сравнете с таблицата в дясно. Тя е официалната таблица за оценяване на МОН.
Доволни ли сте от получения резултат?