Матура по Химия 21 май 2021
Тук можете да решите варианта на матруата по химия от 21 май 2021 година.
За подробна инструкция вижте видеото в дясно.
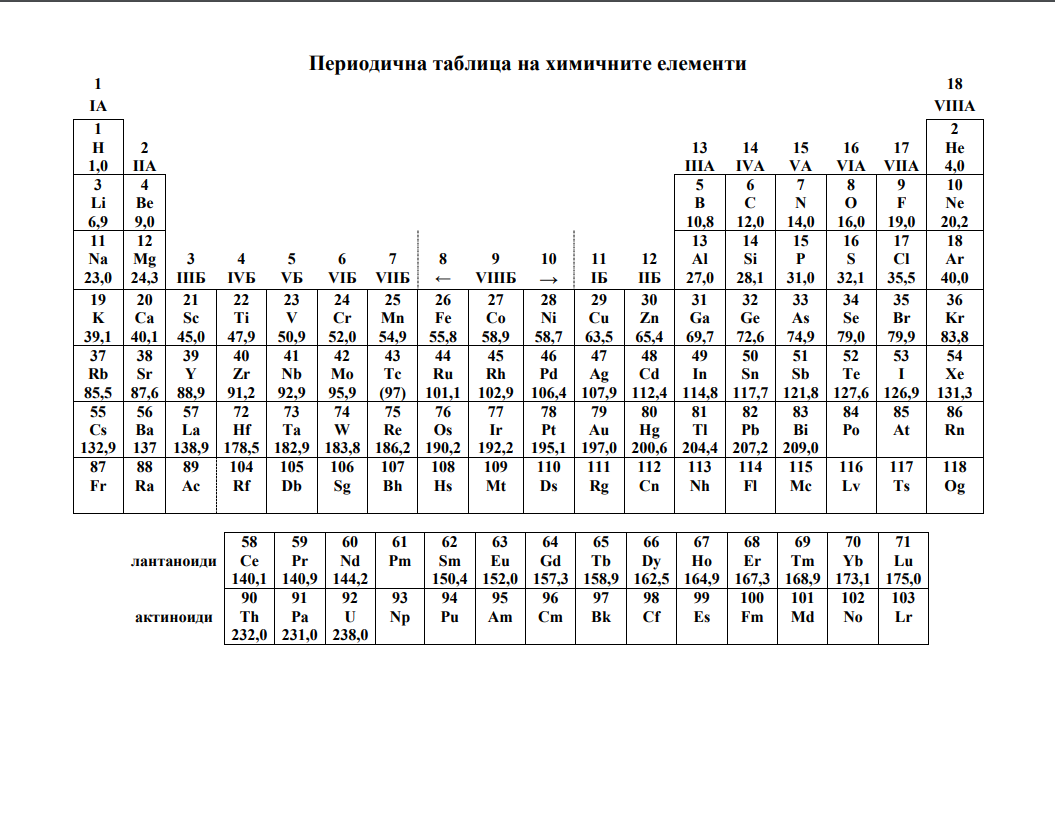
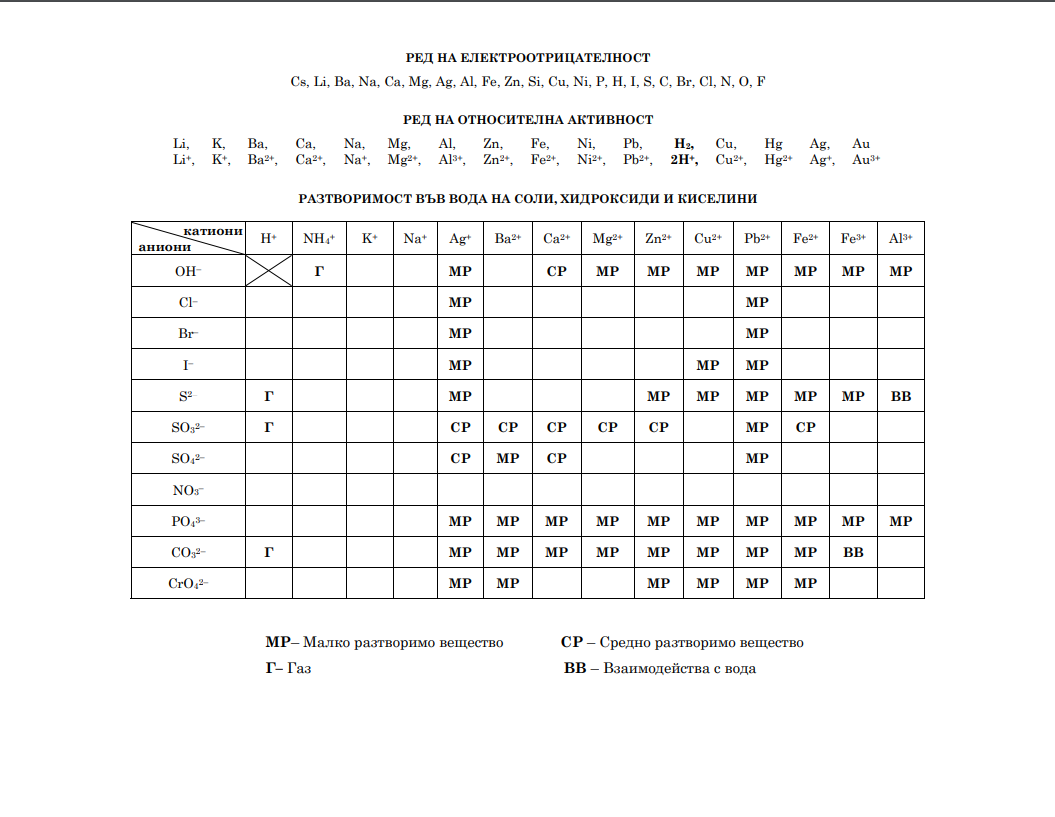
На ваше разположение са помощни таблици, които можете да отворите като кликнете на заглавията долу. Първи модул можете да решите изцяло онлайн. Втори модул няма как да бъде точно оценен автоматично, за това сме ви подготвили въпросите в таблицата в ляво и отговорите в дясно. Решенията записвайте и след това проверете колко точки сте събрали.
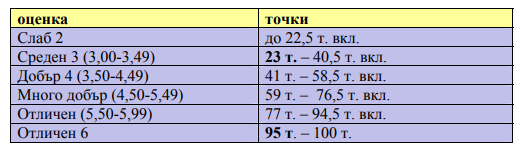
Схемата за оценяване можете да видите в дъното на страницата. Успех!
ПЪРВИ МОДУЛ
Модулът съдържа 35 затворени въпроса с по един възможен отговор. Поради това, този раздел може да бъде оценен автоматично. За всеки верен отговор получавте по една точка. Максимално можете да изкарате 35 точки.Решете теста, запомнете получения брой точки и преминете към втори модул.
ВТОРИ МОДУЛ
Втори модул съдържа задачи с отворен отговор. Тях ще трябва да решите на лист и да оцените самостоятелно според дадения критерий. Запомнене броя точки от първи модул и добавяйте указания брой точки за всеки верен отговор.
За вашата подготовка е най-полезно да дадете вашите отговори преди да започнете да проверявате решенията и да точкувате.
Въпроси
36. Елементът Е се намира в третия период на Периодичната таблица. Простото вещество на Е е сребристосив метал, който гори с ослепително ярка светлина. В получения оксид металните йони са със заряд 2+. Оксидът реагира със солна киселина, при което се получава безцветен разтвор.
А) Напишете химичната формула на оксида на елемента Е.
Б) Изразете с химично уравнение взаимодействието на оксида на елемента Е със солна киселина
37. В реакционния съд А реагират газовете X и Z на един етап по уравнението: X + Z → XZ. В друг съд Б при същите условия (Т и р) в газовата смес е добавен положителен катализатор. Съответните начални коцентрации на X и Z в двата съда са еднакви.
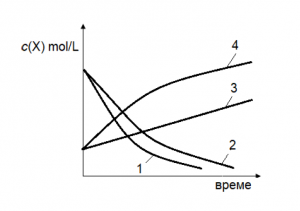
А) В кой съд – А или Б, концентрациите на веществата Х, Z и XZ се променят най-бързо?
Б) Коя от кривите 1, 2, 3, 4 се отнася за реакцията в съд А и коя – за реакцията в съд Б?
38. Цветарка приготвя за наторяване разтвор от 300 g NaNO3 и 2700 g вода.
А) Колко мола NaNO3 се съдържат в получения разтвор? (Закръглете резултата до десети.)
Б) Колко е масовата част на разтвора?
Цветарката разрежда разтвора, като добавя 750 g вода.
В) Колко е масовата част на разтвора след разреждането?
39. Във воден разтвор с рН < 3,1 индикаторът метилоранж е
розов, а при рН > 4,4 – жълт. Фенолфталеинът е малиновочервен при рН > 10, а при рН < 8 е безцветен. В две
чаши има разтвори на HCl (чаша № 1) и NaOH (чаша № 2) с
концентрации 1 mol/L. В чаша № 1 се добавят няколко
капки разтвор на метилоранж, а в чаша № 2 – на
фенолфталеин.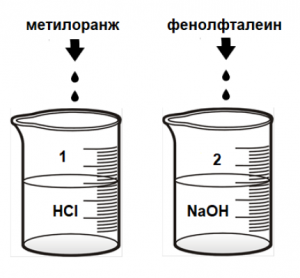
А) Какъв е цветът на разтвора в чаша № 1 и какъв – в чаша № 2,
след прибавяне на индикаторите?
Б) Ако се смесят равни обеми от двата разтвора и се добавят
няколко капки фенолфталеин, какъв цвят ще има полученият
разтвор?
40. K2SO4 е сол, която може да се получи от калиева основа, с химична формула (–-(1)–-) и
–-(2)–- киселина, с химична формула (–-(3)–-). Наименованието на солта K2SO4 e
дикалиев –-(4)–-.
В свитъка за свободните отговори срещу (2) и (4) запишете липсващите думи от наименованията, а срещу (1) и (3 ) – съответните химични формули
41. При взаимодействие на всяко от твърдите вещества: магнезий, меден карбонат и калциев
оксид със сярна киселина (20 %), се получава сол.
Изразете с химични уравнения взаимодействието на всяко от трите твърди вещества със сярна киселина.
42. При термично разлагане на варовик освен въглероден диоксид, се получава веществото А, от
което след взаимодействие с веществото Б се получава веществото В, известно в практиката като
гасена вар.
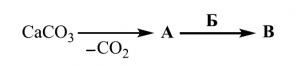
Кои са веществата А, Б и В на схемата с химичните превръщания? Запишете химичните формули на А, Б и В в свитъка за свободните отговори.
43. Кои от твърденията сa верни и кои – неверни? В свитъка за свободните отговори срещу буквите
от А) до Е) запишете ДА или НЕ.
А) Зелените водорасли се нуждаят от CO2.
Б) В черупките на яйцата се съдържа СаСО3.
В) Във въздуха, който човек издишва, се съдържа около 1 об.% Н2.
Г) Киселинните дъждове се причиняват от оксиди на сярата и азота.
Д) В природата сярата се намира само под формата на химични съединения.
Е) Съединението NaHCO3 се използва при приготвянето на тестени храни като набухвател.
44. За всяко наименование в колона I посочете съответстващата му формула в колона II.
Отговорите запишете в свитъка за свободните отговори, като срещу буквите А, Б, В и Г от Колона I запишете съответната цифра от Колона II.
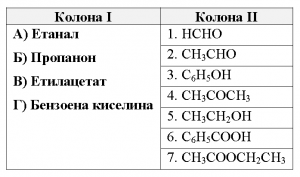
45. От структурните формули от (1) до (6) изберете по две, които изобразяват:
А) хомолози
Б) верижни изомери
В) позиционни изомери
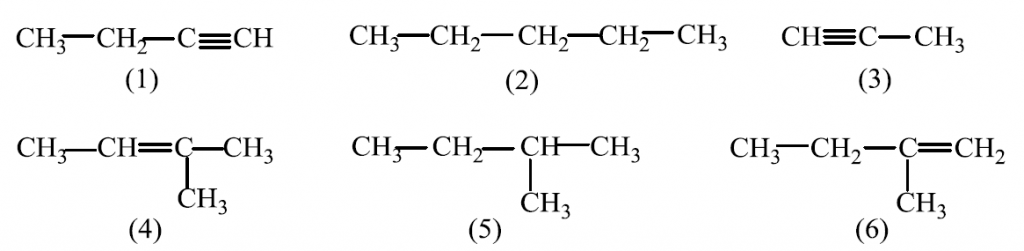
Запишете двойките съединения със съответстващите им номера от (1) до (6) в свитъка за
свободните отговори.
46. Структурните формули от (1) до (6) изобразяват органични съединения, принадлежащи към различни класове.
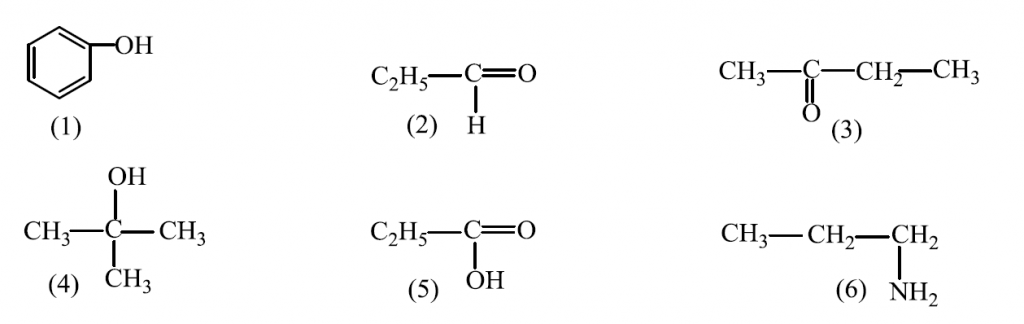
Изберете по едно съединение, което е:
А) амин
Б) фенол
В) кетон
Г) алкохол
В свитъка за свободните отговори срещу съответния клас съединениия от А) до Г) запишете цифрата (от 1 до 6) за избраното съединение.
47. Синтетичен етилов алкохол се получава чрез присъединяване на вода към етен. При
каталитично дехидрогениране на получения етилов алкохол се получава ацеталдехид.
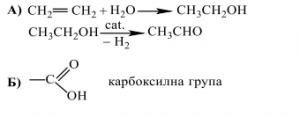
А) Изразете с химични уравнения процесите на получаване на етилов алкохол от етен и на ацеталдехид чрез каталитично дехидрогениране на етилов алкохол.
При окисление на ацеталдехид се получава оцетна киселина.
Б) Изразете със структурна формула функционалната група на оцетната киселина и напишете наименованието на тази група.
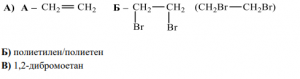
48. Схематично е представен преход с междинен продукт химичното съединение А и краен
продукт съединението Б:
А) Изразете със съкратени структурни формули съединенията А и Б.
Б) Как се нарича продуктът, получен при полимеризация на веществото А?
В) Напишете наименованието на веществото Б според номенклатурата на IUPAC.
49. Изберете подходящите думи и изрази, с които трябва да се допълни текстът.

В двигателите с вътрешно горене от горивото и въздуха се образуват токсични газове, между които
въглероден оксид и азотен оксид. Въглеродният оксид се получава при _____(1)_____ окисление на _____(2)_____. Навън във въздуха азотният оксид се окислява до _____(3)_____, който при подходящи
условия може да причини фотохимичен смог и киселинен дъжд.
В свитъка за свободните отговори срещу (1), (2) и (3) запишете съответните думи или изрази
50. На графиката са представени експериментални данни за разтворимостта на NaNO3 във водапри различни температури
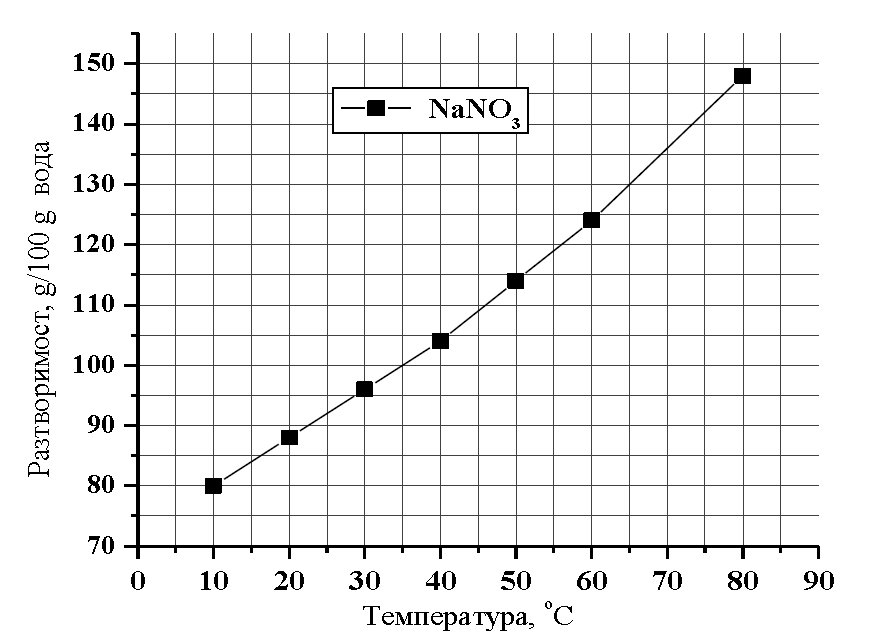
А) Като използвате графиката, определете разтворимостта на NaNO3 (g/100 g вода) при:
(а) 10 °С и (б) 65 °С.
Б) Какъв разтвор ще се получи – ненаситен, наситен или преситен, ако при 10 °С в 200 g вода се
разтворят 150 g NaNO3?
В) Разтворът от т. Б) се нагрява до 65 °С. Колко грама NaNO3 трябва да се добавят към този разтвор, за да се получи наситен разтвор за 65 °С?
Правилни отговори и точки
А) MgO – 1 т.
Б) MgO + 2HCl → MgCl2 + H2O – 2 т.
А) в съд Б – 1 т.
Б) крива 2 – съд А; крива 1 – съд Б – 2 х 1 т.
А) 3,5 mol NaNO3 – 2 т.
Б) 0,10 (10 %) Б) – 1 т.
В) 0,08 (8 %) – 1 т
А) № 1– розов № 2 – малиновочервен – 2×1=2 т.
Б) няма цвят или безцветен – 1 т.
(1) – KOH – 1 т.
(2) – сярна – 1 т.
(3) –H2SO4 – 1 т.
(4) – сулфат – 1 т.
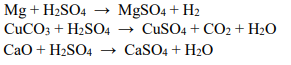
Макс. 3×2=6 т.
А – CaO – 2 т.
Б – H2O – 2 т.
B – Ca(OH)2 – 2 т.
А) Да – 1 т.
Б)Да – 1 т.
В)Не- 1 т.
Г)Да – 1 т.
Д)Не- 1 т.
Е)Да – 1 т.
Макс. 6т.
А) – 2 – 1 т.
Б) – 4 – 1 т.
В) – 7 – 1 т.
Г) – 6 – 1 т.
Макс 4т.
А) (1) и (3) – 1 т.
Б) (2) и (5) – 1 т.
В) (4) и (6) – 1 т.
А)– 6 – 1 т.
Б) – 1 – 1 т.
В) – 3 – 1 т.
Г) – 4 – 1 т.
А) 2×2=4 т.
Б) 2×1=2 т.
Макс: 6 т.
А) 2×2=4 т.
Б) 1 т.
В) 1 т.
Макс: 6 т
(1) – непълно – 1 т.
(2) – горивото – 1 т.
(3) – азотен диоксид – 1 т.
А) (а) 80 g/100 g вода (б) 130 g/100 g вода – 2 х 1 т.
Б) ненаситен – 1 т.
В) 110 g – 1 т.
Резултат
Сега е момента да направите изчислението. Към точките от първата част доббавете точките от втората, която решихте на лист. Сравнете с таблицата. Тя е официалната таблица за оценяване на МОН.
Доволни ли сте от получения резултат?